2021年6月10日,我院于超教授课题组关于开发一种新型的多功能自组装纳米药物以实现乳腺癌的治疗与成像一体化的研究结果在线发表于知名学术期刊ACS Applied Materials & Interfaces上。文章标题:Self-Assembling Porphyrins as a Single Therapeutic Agent for Synergistic Cancer Therapy: A One Stone Three Birds Strategy,学院研究生陈俊、陈凤、张磊为共同第一作者,于超教授为通讯作者。

根据2020年全球癌症患者的数据统计,乳腺癌已超越肺癌成为全球新发癌症患者数排名第一的恶性疾病,严重威胁人类生命健康安全。传统的乳腺癌治疗手段主要分为三大类:手术切除,化疗和放疗,然而其存在的侵入性和全身性毒副作用,影响患者的治疗与预后效果。诊疗一体化纳米技术因其具有良好的成像能力及高效递送水平和较好的疾病治疗效果,在抗肿瘤药物设计领域受到广泛关注。
然而,现有的纳米诊疗系统对于肿瘤组织的时空特异性效应的局限性,使其高效治疗和精准成像的目标难以实现。因此,设计解决时空可控的高效诊疗一体化系统成为纳米药物研究的迫切需求。光动力学疗法因其具有时空可控的本征特性,在临床疾病治疗和临床前研究中应用广泛。但是,单一疗法的使用已不能满足临床有效治疗癌症的需求,因此,多模态治疗策略成为研究人员治疗肿瘤的主要手段之一。而如何制备具有多模态治疗功能的单一治疗剂给研究人员提出了尚待解决的难题。自组装纳米技术为解决这一问题提供了契机,其通过将各含不同功能的分子单体,利用共价或非共价作用,一步自组装形成单一纳米药物。这类自组装纳米药物通过尺寸效应实现肿瘤组织的有效富集,并在肿瘤部位释放各类功能单体分子,实现肿瘤的多模态治疗。
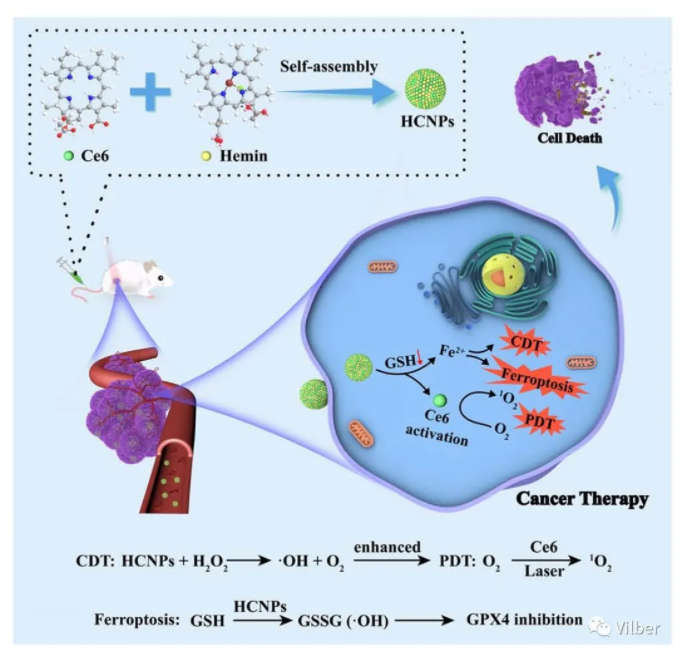
于超教授课题组开发的新型多功能自组装纳米药物,通过简单一步自组装方式,将二氢卟吩e6和氯化血红素结合形成新型的纳米药物。利用二氢卟吩e6的荧光特性,可实时监测纳米药物在体内分布情况。与单独的二氢卟吩e6及对照组相比,纳米药物组在体内循环时间更长,并能够有效蓄积在肿瘤部位且停留较长时间。